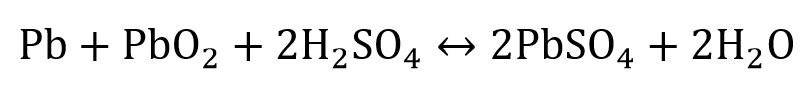محصولات بازدید شده
فید RSS
هیچ فید RSS اضافه نشده است
شاخه های بلاگ خبری
Latest contents

باتریهای سربی – اسیدی اولین و پرکاربردترین تکنولوژی باتری در وسایلنقلیه میباشد. این باتریها برای بیش از یک قرن یک محصول تجاری موفق بوده و با داشتن مزایایی همچون قیمت پایین، تکنولوژی رشد یافته و توان نسبتاً بالا بهصورت گستردهای در زمینه خودرو و دیگر کاربردها بکار رفته است.
نکته: باتری سربی – اسیدی در سال 1859 توسط فیزیکدان فرانسوی به نام گاستون پلانته اختراع شد.
نحوۀ عملکرد این باتریها را میتوان بهصورت ذیل تشریح کرد.
هرگاه دو فلر غیر هم جنس درون محلول اسیدی یا الکترولیت قرار گیرند، جریان برق تولید میشود. به طوری که یک از این دو فلز الکترون میدهد (صفحۀ منفی) و دیگری الکترون میگیرد (صفحۀ مثبت). میزان ولتاژ تولیدی به جنس دو فلز و نوع الکترولیت دارد.
نکته: اگر دو فلز غیر هم جنس طلا و آلومینیوم بهعنوان صفحات باتری انتخاب شوند، بیشترین مقدار ولتاژ تولید میگردد.
اگر دو فلز غیر هم جنس، یکی از جنس سرب (Pb) بهعنوان صفحۀ منفی و دیگری از جنس دی اکسید سرب (Pbo2) بهعنوان صفحۀ مثبت در محلول آب (H2O) و اسید سولفوریک (H2SO4) قرار گیرد، باتری سربی – اسیدی تشکیل شده که حداکثر 2.2 ولت برق تولید میکند.
شکل ذیل وضعیت باتری در دو فرایند تخلیه و شارژ را نشان داده است. در فرایند تخلیه (استفاده از برق باتری) به تدریج سولفات (SO4) از الکترولیت جدا شده و به صفحۀ مثبت و منفی میچسبد و از طرفی اکسیژن (O2) صفحۀ مثبت نیز از این صفحه جدا شده و وارد الکترولیت میشود. چنانچه این روند به مدت زیادی ادامه یابد. جنس صفحۀ مثبت و منفی به سولفات سرب (PbSO4) و الکترولیت به آب تبدیل میشود.
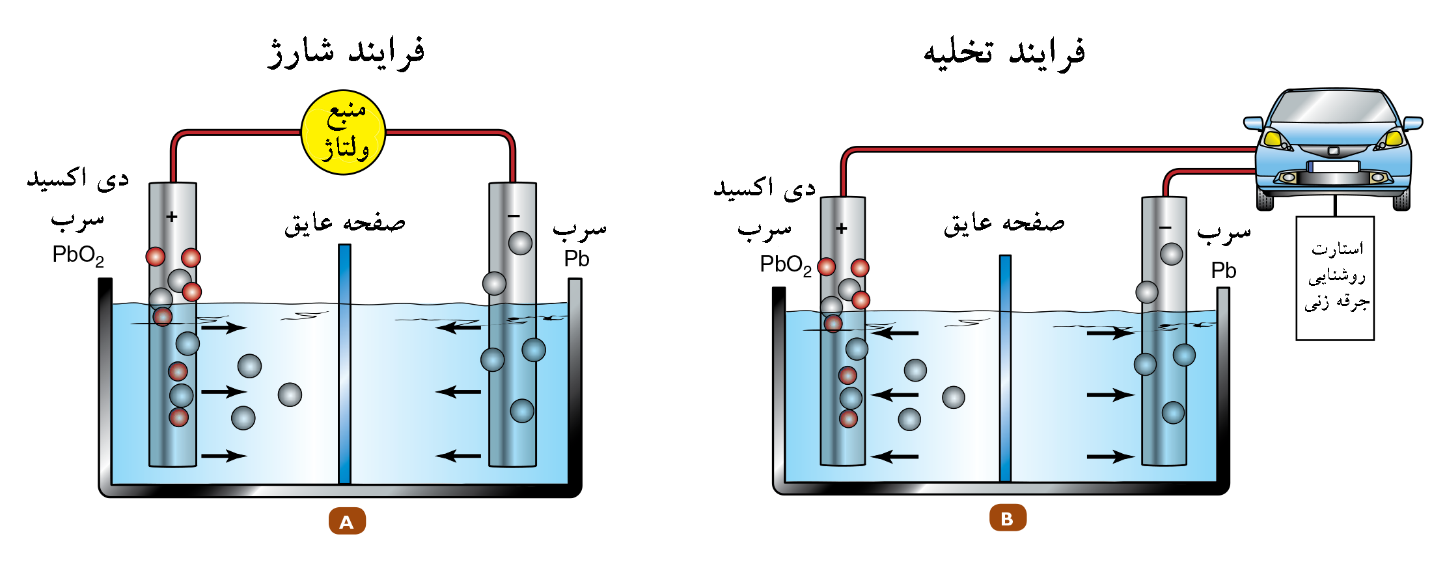
در فرایند شارژ باتری، حالتی معکوس صورت میگیرد. بهعبارت دیگر شارژ باتری روندی است که سولفاتهای (SO4) چسبیده شده به صفحۀ مثبت و منفی از صفحات جدا شده و وارد الکترولیت میشوند و اکسیژن (O2) به صفحۀ مثبت باز می گردد.
فرمول شیمیایی دو فرایند تخلیه و شارژ در یک باتری سربی – اسیدی را میتوان بهصورت ذیل نشان داد.
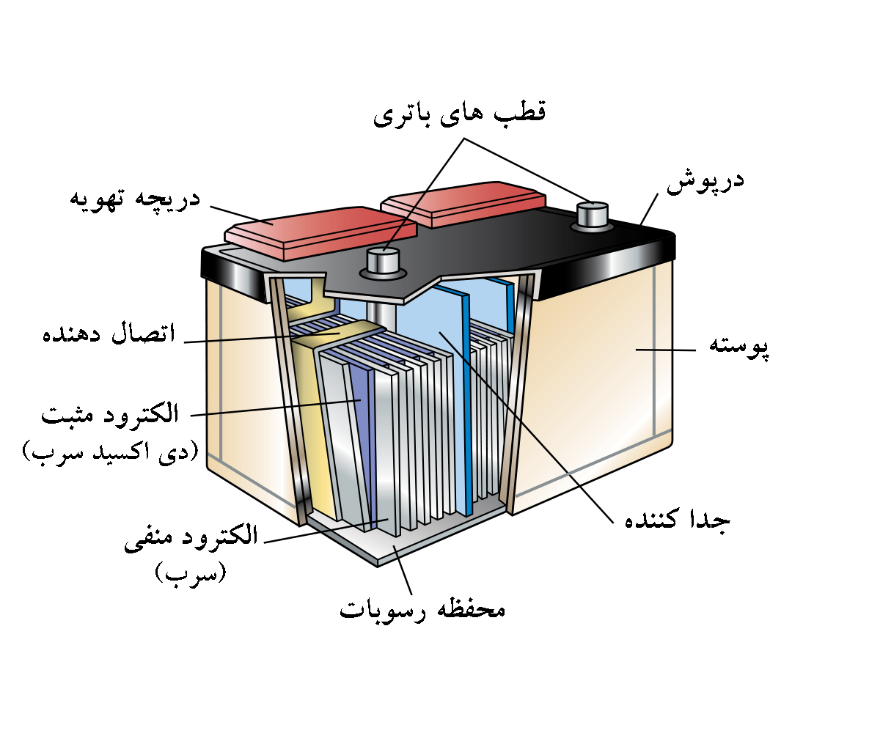
شکل ذیل اجزای یک باتری سربی – اسیدی را نشان داده است.